一、体重多少算超重/肥胖?
身体质量指数(Body mass index,BMI):体质量(kg)/身高(m)2,可用来间接评估人体的脂肪成分,是国际上测量与诊断超重和肥胖使用最广泛的指标,腰围、腰臀比、腰围身高比:反映中心性肥胖的间接测量指标,可用于预测疾病发生率和死亡率;
皮褶厚度:可用于间接评估身体脂肪的含量及分布。
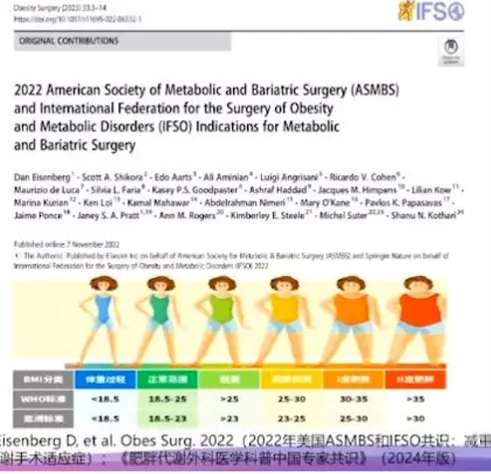
超重/肥胖:● WHO分类标准:25 kg/m2≤BMI<30 kg/m2;BMI≥30 kg/m2为肥胖;● 中国分类标准:24kg/m2≤BMI<28kg/m2为超重;BMI≥28kg/m2为肥胖。《中国居民肥胖防治专家共识》(2022年):WHO BMI classification (June 2021)。
二、肥胖也会影响怀孕几率?
肥胖可导致女性不孕症发生 主要可能机制如下:

● 肥胖的病理生理学基础机制之一是由促炎因子介导的低度全身性炎症;
● 促炎因子包括由脂肪组织分泌的游离脂肪酸、脂多糖、脂肪因子(包括瘦素、内脂素)和细胞因子(TNF-α、IL-1β、1L-6)等;
● 促炎因子与肥胖引起的胰岛素抵抗和高雄激素血症共同作用,加剧的免疫反应对下丘脑-垂体-性腺轴的各个层面产生负面影响,导致卵巢功能絮乱,月经周期不规则和无排卵,最终导致不孕症。

2022年南京医科大学研究成果:肥胖对卵子及早期胚胎发育的影响
● 肥胖会引起卵母细胞内脂毒性,增加了内质网应激并损害内质网及线粒体细胞信号传导,导致细胞凋亡,最终导致卵母细胞和早期胚胎发育异常;
● 动物研究发现母源肥胖导致卵母细胞内去甲基保护因子(Stella)显著减少,受精后雌原核内双加氧酶(TET3)介导的5-羟甲基胞嘧啶(5hmC)的异常积累,最终导致早期胚胎发育阻滞。


●Zhang等一项回顾性队列研究对22043个首次FET周期进行分析,发现母体肥胖与胚胎植入率、临床娠率和活产率降低有关;
●Sutaji等发现PCOS女性子宫内膜肝素结合性表皮生长因子(Hb-EGF)表达低于正常体重PCOS女性;
●肥胖引发的炎症和致瘤环境增加子宫内膜病变风险(脂肪组织中FFA和炎性细胞因子分泌增多,脂联素分泌减少,炎症介质从循环中吸引中性粒细胞、Th1淋巴细胞、单核细胞等促进炎症环境,增加ROS的产生,高水平的ROS和炎症信号可能导致组织的恶性转化)。
三、备孕期间如何健康减肥,轻松怀上?

饮食干预
● 限能量饮食 在限制能量摄入(日常饮食能量减去30%)的基础上营养素比例符合各类人群平衡膳食的要求。
● 高蛋白饮食 每日蛋白质摄入量超过20%,但一般不高于35%的膳食模式,适应于肾功能正常且需要短期快速减重的伴有糖脂代谢异常的人群。
● 代餐饮食
满足成年人控制体重期间一餐或两餐的营养需要代替一餐或两餐,专门加工配制而成的一种控制能量食品,大部分具有低热量、高纤维性、易饱腹的特点。
● 极低能量饮食 每日仅摄入600-800kcal能量饮食,保持蛋白质和碳水化合物的最低需要量,适用于重度肥胖症快速减重治疗,仅短期应用。
● 低碳水化合物饮食 目前尚无碳水化合物供能比的统一标准,一般在20-40%,<20%为极低碳水化合物饮食,仅短期应用。
●低脂饮食 目前尚无脂肪供能比的统一标准,一般在20-25%。
● 轻断食模式也称间歇性断食: 一般采用5+2模式,1周中5天相对正常进食其他2天(非连续)则摄取平常的1/4能量(男性600kcal/d,女性500kcal/d)的膳食模式。
运动干预
● 运动是减重治疗中不可或缺的一部分,可通过减少脂肪成分,增加肌肉含量;
● 主动运动是肥胖症运动干预的重要措施,应以注重患者安全为原则,制定个性化运动处方;
●有氧耐力运动:建议超重或肥胖者每天累计达到60~90 min中等强度有氧运动(如快走、慢跑、游泳等),每周5~7d;
●力量抗阻训练:中等强度抗阻肌肉力量锻炼(如举哑铃、俯卧撑等)隔天进行,每次10~20 min,每周2-3次;
● 提倡增加体力活动与适当控制膳食总能量相结合,促进能量负平衡。

药物干预
● 对于超重/肥胖并伴有体重相关并发症的人群,若生活方式干预减重效果不佳,建议增加抗肥胖药物(AOMs)干预。
● 对于大多数患者肥胖的长期治疗,首选司美格鲁肽(2.4mg)或利拉鲁肽(3.0 mg),可调节血糖,治疗2型糖尿病。
● 对于伴有偏头痛的患者,可选用芬特明/托吡酯缓释制剂,但托呲酯有致畸作用,不建议备孕女性使用。
● 对于合并抑郁症超重/肥胖患者,可选用纳洛酮缓释/安非他酮缓释制剂。
● 因奥利司他减肥效果较小且有胃肠道副作用,对于超重/肥胖并伴有体重相关并发症的人群不建议使用。
● FDA批准芬特明单药或安非拉酮单药可用于短期治疗肥胖(12周)。
减重手术
● 30 kg/m2 ≤BMI≤34.9 kg/m2 在手术治疗前可先尝试非手术治疗,如饮食控制、药物治疗等,对于非手术治疗无效的人群,应建议行减重代谢手术(MBS)治疗。
● BMI≥35 kg/m2 无论是否存在肥胖相关合并症,都应强烈建议此类人群行MBS。
● BMI≥60 kg/m2 针对极端肥胖人群的最佳手术方式虽尚未达成共识,但MBS对于此类人群有效且安全,应作为减重的首选方式。
● 亚洲人群 亚洲人群低BMI个体的糖尿病和心血管疾病的发生率高于非亚洲人群,BMI≥27.5 kg/m2 的人群应考虑行MBS。
PCOS患者体重管理

生活方式干预减重可恢复排卵性月经周期并减少代谢风险,对大多数超重/肥胖不孕女性而言是一线干预措施。
体重管理一高龄/卵巢功能减退 ;与正常体重相比,超重和肥胖女性CLBR较低。2023年一项多中心回顾性队列研究,2013年1月至2018年2月在18个生殖中心首次IVF/ICSI周期,共14213名患者,
BMI被细分为以下亚组:
①低体重指数(<18.5 kg/m2)②正常体重(18.5-24.9 kg/m2)③超重(25.0-29.9 kg/m2)④ 肥胖(30.0 kg/m²)
●1年内将BMI从肥胖降至超重或超重降至正常体重可能对35岁以下的人有益,而只有大幅降低(即从肥胖降至正常BMI)对36-38岁的女性才有潜在的益处。
●在38岁以上,即使是相当大的体重减轻也无法弥补1年内年龄的影响
●在3个月的时间内,33岁以下的女性BMI降低1kg/m2,33.5-35.5岁的女性BMI减少2 kg/m2,35.75至37.25岁的女性BMI减少3kg/m2,37.50至39.00岁的女性BMI减少4 kg/m2,39.25岁以上的女性BMI减少5kg/m2或更多,才可能对CLBR有益。
辅助助孕前1年内的减重有潜在益处,尤其是在BMI为25 kg/m2的35岁以下女性中,对于35岁以上的人群来说,减重应该更大幅度或在更短的时间内进行,以避免女性年龄增长对其活产的负面影响。

年龄<35岁合并卵巢储备功能低下
● 窦卵泡计数(AFC)<5,抗苗勒管激素(AMH)<1.2μg/L,单纯性超重/肥胖患者,建议减重5%~10%;伴有以肥胖为基础的合并症,纠正代谢指标至正常后助孕。
● 年龄≥35岁合并卵巢储备功能低下 单纯性超重/肥胖患者减重的同时进行助孕治疗;伴有以肥胖为基础的合并症,应纠正代谢指标至正常,减重的同时进行助孕治疗。
● 年龄≥35岁合并卵巢储备良好(AFC≥5,AMH≥1.2μg/L),减重的同时进行助孕治疗。
备注以上内容出自:生殖健康新探索风险防控与创新诊疗 相关内容
更多备孕干货内容:
肥胖备孕对孩子有影响吗?肥胖对备孕女性 IVF / ICSI-ET 妊娠结局的影响

